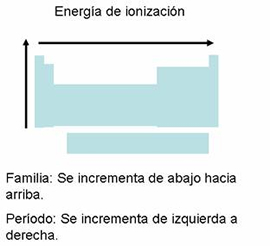
Energía o potencial de ionización
Es la cantidad de energía que se requiere para eliminar el electrón más débilmente unido al átomo. La energía de ionización en los periodos aumenta de izquierda a derecha y en los grupos, aumenta de abajo hacia arriba.
Dos factores influyen sobre el potencial de ionización. Por una parte será mayor cuanto más atraído esté el electrón que se pierde por el núcleo atómico. Por otro lado, como los átomos tienden a tener ocho electrones en su capa de valencia, acercarse a este ideal disminuirá el potencial de ionización, y alejarse de él lo aumentará.